AG Geweberegeneration
AG Geweberegeneration
Die Arbeitsgruppe Geweberegeneration unter der Leitung von PD Dr. Anika Jonitz-Heincke erforscht am Forschungslabor für Biomechanik und Implantattechnologie (FORBIOMIT) der Universitätsmedizin Rostock zelluläre und molekulare Mechanismen der Knochen- und Knorpelregeneration. Ziel ist es, aus grundlagenwissenschaftlichen Erkenntnissen neue Strategien für die Behandlung von Gelenkerkrankungen, Knochendefekten und Implantatversorgungen abzuleiten. Die Arbeitsgruppe ist in mehrere große interdisziplinäre Forschungsverbünde eingebunden.
Zellbiologische Expertise und Primärzellkulturen
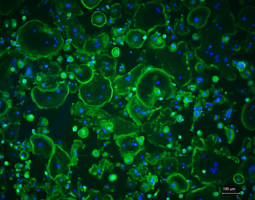
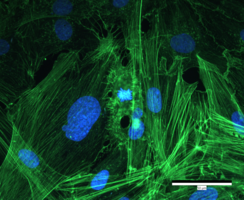
Die Arbeitsgruppe verfügt über umfangreiche Erfahrungen in der Isolation und Kultivierung humaner Primärzellen, die aus u. a. aus Hüftköpfen, hyalinem Gelenkknorpel sowie Buffy Coats und Vollblut gewonnen werden. Diese Zellen bilden die experimentelle Grundlage für nahezu alle Forschungsprojekte der AG und ermöglichen es, biologische Fragestellungen unter physiologisch relevanten Bedingungen zu untersuchen. Die Kultivierung erfolgt sowohl in zweidimensionalen Monolayern als auch in dreidimensionalen Kultursystemen, die die natürliche Gewebeumgebung besser abbilden. Zu den etablierten Primärzellkulturen zählen Osteoblasten, Osteozyten, Osteoklasten und Chondrozyten sowie Fibroblasten und PBMCs. Diese Bandbreite an Zelltypen ermöglicht der AG, sowohl die Knochen- und Knorpelregeneration als auch entzündliche Prozesse auf zellulärer Ebene zu adressieren.
Elektrische Stimulation zur Knochen- und Knorpelregeneration
Ein zentraler Forschungsschwerpunkt der AG ist die gezielte Nutzung elektrischer Felder zur Förderung der Geweberegeneration. Die Arbeiten sind im DFG-Sonderforschungsbereich 1270 „ELektrisch Aktive ImplaNtatE – ELAINE“ eingebettet.
Endogene elektrische Potenziale spielen eine zentrale Rolle bei der natürlichen Geweberegeneration. Die AG untersucht, wie sich elektrische Wechselfelder therapeutisch einsetzen lassen, um zwei wesentliche klinische Herausforderungen zu adressieren: die Reparatur von Knorpeldefekten und die Verbesserung der Osseointegration von Implantaten.
Für die Regeneration von hyalinem Knorpelgewebe erfolgen elektrische und mechanische Stimulationsversuche mit humanen Knorpelzellen in Monolayer-Kulturen oder in Hydrogel-basierten Gerüststrukturen. Als Zielparameter werden die Zellmorphologie, die Viabilität sowie die Deposition von Kollagen Typ I und Typ II analysiert, wobei das Verhältnis von Kollagen Typ II zu Typ I als Maß für die Redifferenzierungskapazität dient. Die Untersuchungen berücksichtigen zudem geschlechtsspezifische Unterschiede in der zellulären Antwort, die für die Entwicklung personalisierter Therapieansätze relevant sein könnten.
Im Bereich der Knochenregeneration untersucht die AG in vitro die Wirkung alternierender elektrischer Felder auf osteogene und osteoklastische Zellen in Langzeitversuchen. Die zellulären Antworten variieren in Abhängigkeit von Spannung und Frequenz, wobei die Elektrostimulation die osteogene Differenzierung und Mineralisierung wesentlich fördert. Ziel ist es, auf Basis dieser In-vitro-Daten therapeutische Fenster für eine optimierte elektrische Stimulation der Knochenregeneration zu definieren.
Materialinduzierte Entzündungsreaktionen
Ein weiterer Schwerpunkt der AG liegt auf den molekularen Mechanismen partikelinduzierter Entzündungsprozesse, wie sie bei der aseptischen Lockerung von Gelenkendoprothesen auftreten. Diese Forschung ist Teil des DFG-Graduiertenkollegs 2901 „Systemische und lokale Reaktionen bei Unverträglichkeiten gegenüber Biomaterialien für Gelenk- und Hautläsionen – SYLOBIO“.
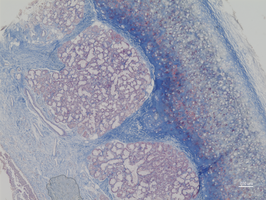
Metallische Abriebpartikel, die durch den Verschleiß künstlicher Gelenke entstehen, werden von knochenaufbauenden Osteoblasten aufgenommen und lösen eine komplexe Entzündungskaskade aus. Unsere Arbeiten zeigen, dass die Partikelaufnahme bereits kurz nach dem Erstkontakt über Veränderungen der Zellmorphologie und spektraler Daten nachweisbar ist und unmittelbar eine molekulare Antwort auslöst. Mithilfe zeitaufgelöster Genexpressionsanalysen identifizieren wir relevante Expressionsprofile von Oberflächenrezeptoren und assoziierten intrazellulären Signalwegen, die das Zusammenspiel von Partikelexposition und inflammatorischer Aktivierung in Osteoblasten abbilden. Im Zentrum der Entzündungsreaktion steht dabei u. a. das NLRP3-Inflammasom – ein intrazellulärer Proteinkomplex, der als Sensor für Gefahrensignale fungiert und die Freisetzung proinflammatorischer Zytokine wie IL-1β und IL-18 reguliert. Darüber hinaus wird der Einfluss freigesetzter Metallionen auf die Differenzierungskapazität von humanen Knochenzellen untersucht. Methodisch setzt die AG auf Ko-Kulturmodelle, die das Zusammenspiel verschiedener Zelltypen im periprothetischen Gewebe abbilden, und erhebt umfassende OMICs-Daten einschließlich Single-Cell-Analysen, um zelltyp- und patientenspezifische Reaktionsmuster auf molekularer Ebene aufzulösen.
Hydrostatische Hochdruckbehandlung von Gewebetransplantaten
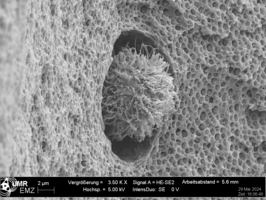
Die Aufbereitung allogener Transplantate mittels konventioneller Verfahren wie Bestrahlung oder chemischer Dekontamination beeinträchtigt häufig die biomechanische Integrität und die induktiven Eigenschaften des Gewebes. Die AG nutzt die hydrostatische Hochdrucktechnologie, um Zellen in muskuloskeletalem Gewebe zuverlässig zu devitalisieren, während die extrazelluläre Matrix erhalten bleibt. Neben umfangreichen Studien zur Devitalisierungseffizienz werden experimentelle Untersuchungen zur Revitalisierung der behandelten Gewebe in vitro und in vivo durchgeführt. Ergänzend werden Protokolle zur mikrobiellen Dekontamination sowie zur onkologisch sicheren Aufbereitung tumorinfiltratierten Gewebes erforscht.
Implantatwerkstoffe
In interdisziplinärer Zusammenarbeit werden neuartige Werkstoffe für die Endoprothetik biologisch charakterisiert, darunter additiv gefertigte Titan-Niob-Tantal-Legierungen mit knochenähnlicher Elastizität sowie Hybridmaterialien aus aluminiumoxidverstärkter Zirkonoxidkeramik und Titanlegierungen oder Tricalciumphosphate.
Projektträger





AG Leiterin
Mitarbeitende
- Dr. rer. nat. Annett Klinder
- Dr. rer. hum. Janine Waletzko-Hellwig
- Dr. rer. hum. Marie-Luise Sellin
- Vivica Freiin Grote, M.Sc.
- Henrike Löffler, M. Sc.
- Irem Simsek, M. Sc.
- Erik Dargel, M. Sc.
- Heinke Plischke, MTA
- Studierende